酰胺是蛋白质组成中的关键连接单元,同时其化合物广泛用作药物和精细化学品合成的原料。5-氰基戊酰胺(5-cyanovaleramide, 5-CVAM)作为催化己二腈(Adiponitrile, ADN)水合反应得到的单酰胺中间产物,是合成新型除草剂唑啶草酮的重要前体物质,具有巨大的工业化应用前景。腈水合酶(Nitrile hydratase,NHase)催化合成路线具有绿色环保、条件温和以及高效等优势,被认为是取代传统化学工业合成5-CVAM的最佳选择。
梁长海教授团队在前期研究中通过优化外源表达过程中RBS序列,实现了对来源于Rhodococcus erythropolis CCM2595的Fe型腈水合酶(ReNHase)α亚基和β亚基的平衡表达,不仅保障了酶结构的完整性,且优化后的ReNHase催化ADN比酶活提高了12倍,催化效率提高了3.75倍(ChemBioChem 2024, 25, e202400526,中国专利ZL 202310433598.2)。然而催化效率的大幅提高也伴随着对5-CVAM区域选择性的明显下降,导致生成副产物己二酰胺(Adipamide, ADM)。
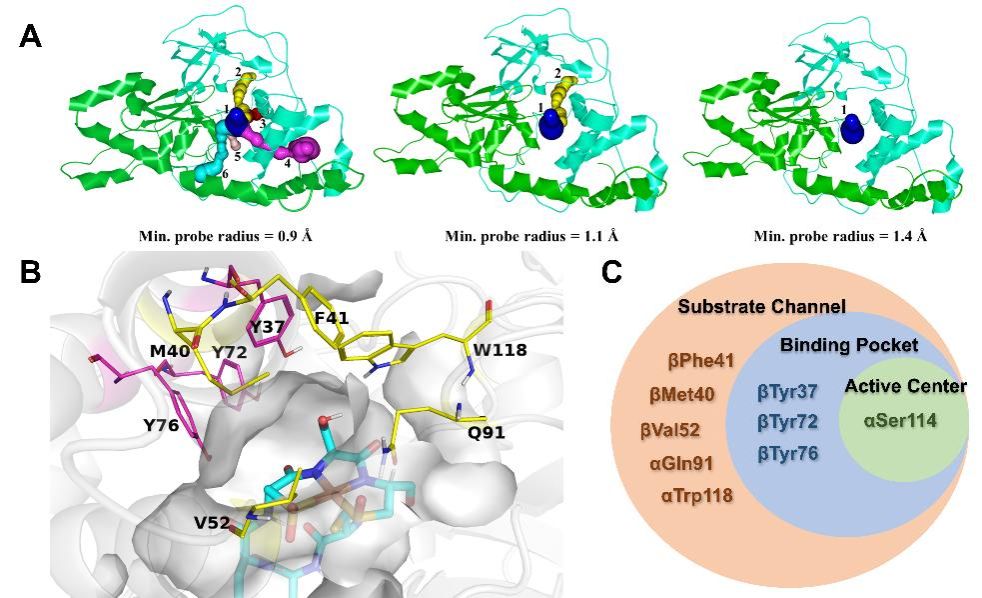
图1 ReNHase底物通道和结合口袋的关键残基预测
针对上述问题,研究团队提出了基于半理性设计的酶工程化改造策略实现对ReNHase区域选择性进行调控。基于半理性设计预测并得到了位于ReNHase底物通道和结合口袋的重要残基,在剔除高度保守和影响酶活性的残基位点后建立了突变体文库。进行筛选并进行酶动力学参数表征后,锁定了能够调控催化ADN反应产物区域选择性的关键位点βTyr72,并且得到了对于5-CVAM区域选择性分别为96%和100%的突变体βY72A和βY72C。
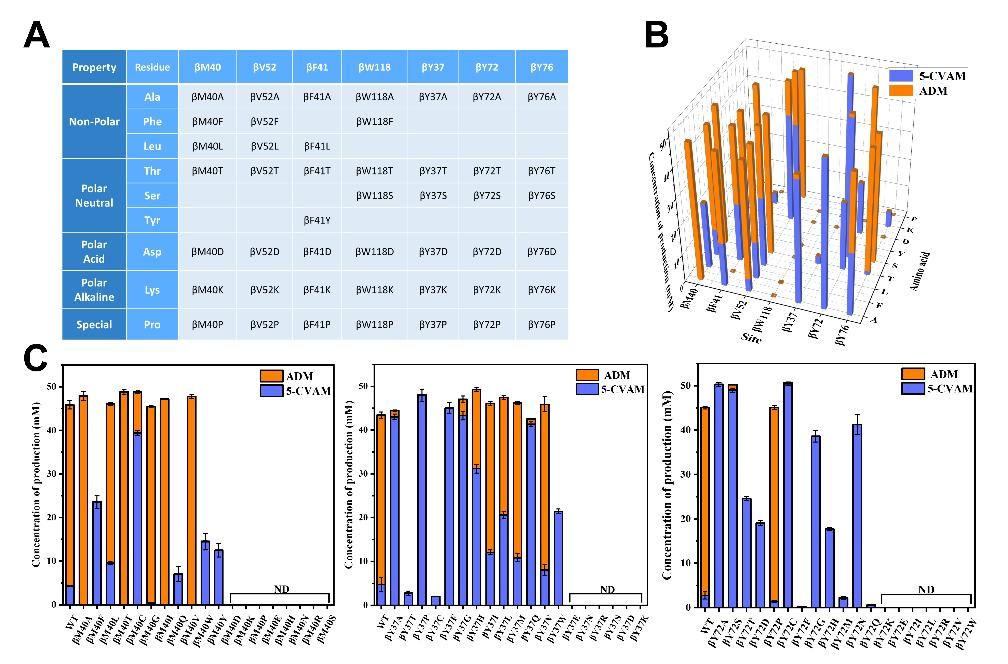
图2 突变文库建立与筛选
再通过对比酶突变前后底物通道的构象变化、结合口袋的体积变化,分子对接与分子动力学模拟对于酶与底物(包括ADN与5-CVAM)之间相互作用的计算分析,详细讨论了两种突变体是如何通过影响酶自身结构以及与底物之间的相互作用,实现了对5-CVAM区域选择性的提升。
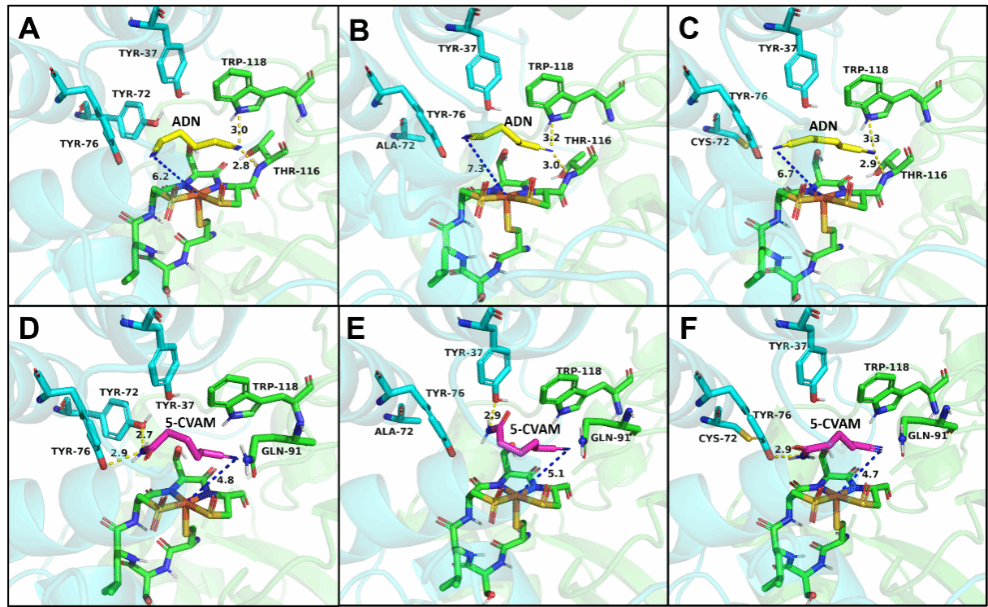
图3 野生型ReNHase及突变体同底物ADN/5-CVAM的分子对接
在此基础上进一步深入揭示了βTyr72作为重要的“开关”残基,在对调控己二腈水合反应产物的区域选择性以及酶催化活性这两个方面的关键作用与结构学意义。
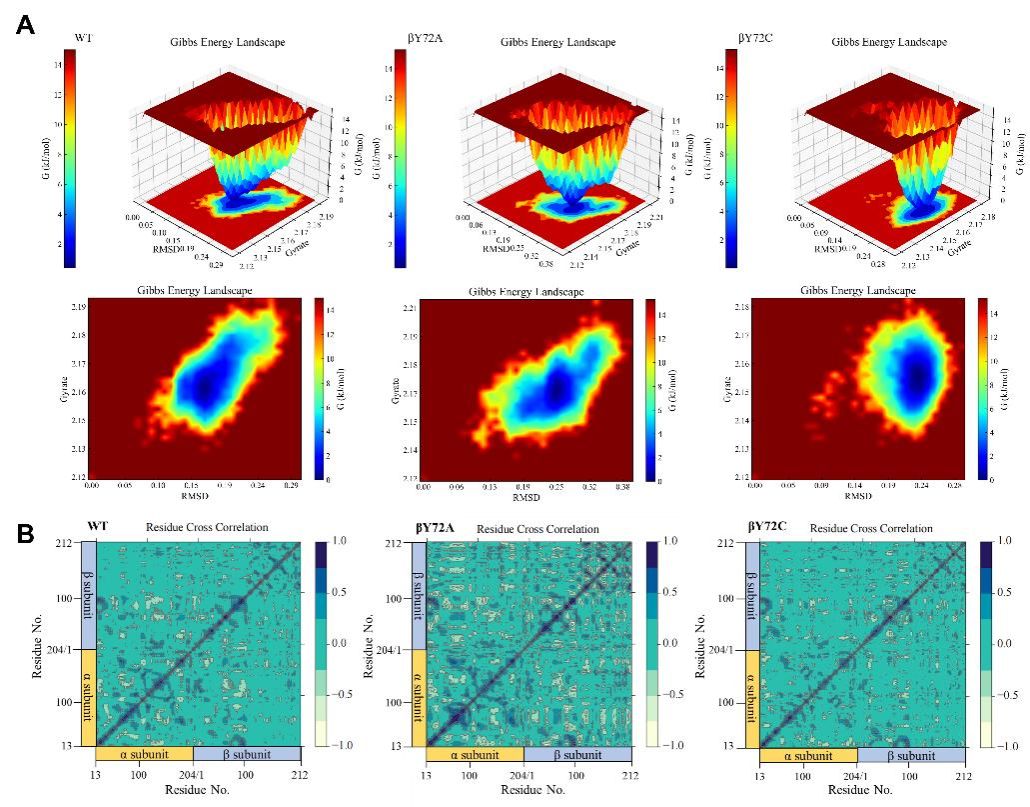
图4 自由能景观(FEL)和动态互相关矩阵(DCCM)分析
相关结果近日以Reprogramming Regioselectivity of Nitrile Hydratase towards Adiponitrile via Semi-rational Design of a Key “Switch” Residue为题发表在生物学领域知名期刊International Journal of Biological Macromolecules(2026, 357, 151582)上。论文第一作者为博士研究生郭祎,通讯作者为梁长海教授与王黎副教授。同时相关结果已获得中国发明专利授权(一种调控腈类化合物区域选择性的腈水合酶改造方法与应用,ZL 2024 1 1198452.5)。目前相关菌株已用于在大连理工大学成都研究院进行的5-氰基戊酰胺生物制造的放大验证,获得了重要进展。
上述研究工作得到辽宁省“兴辽英才计划”(XLYC1908033)、中央高校基本科研业务费专项基金(DUT2021TD103, DUT23YG121)以及大连理工大学成都研究院的资助。
